Ewing sarcoom
Deze informatie is opgesteld door de afdeling(en) Orthopedie.
Wat is Ewing sarcoom?
Het Ewing-sarcoom is een kwaadaardige bottumor, een vorm van botkanker. De tumor ontstaat in het bot (geen uitzaaiing van een andere vorm van kanker), maar kan ook voorkomen in de weke delen (spieren en bindweefsel). Professor James Ewing heeft deze bottumor voor het eerst beschreven begin 19e eeuw, en daaraan ontleent de tumor zijn naam. Een Ewing-sarcoom kan in het hele lichaam voorkomen, zowel in platte botten (het bekken en de ribben) als ook in de pijpbeenderen (het dijbeen, scheenbeen en de bovenarm). Het Ewing sarcoom is zeldzaam, maar na het osteosarcoom de tweede meest voorkomende vorm van botkanker. In Nederland zijn er ongeveer 30-35 nieuwe patiënten per jaar. De leeftijdspiek ligt tussen de 10 en 20 jaar. Een Ewing-sarcoom komt iets vaker voor bij jongens/mannen dan bij meisjes/vrouwen (verhouding 1,5:1).
Verschijnselen
Indien er klachten zijn is één van de eerste klachten pijn, meestal s’ nachts. De pijn zit meestal rondom de tumor. Soms treedt er een zwelling op. Als de tumor zich dicht bij het gewricht bevindt kan er een functiebeperking ontstaan. Tevens kan een spontane botbreuk optreden door de aantasting van het bot. De duur van de symptomen is wisselend, van enkele weken tot enkele maanden. Algemene verschijnselen kunnen moeheid, gebrek aan eetlust, gewichtsverlies en koorts zijn.
Oorzaak
Het is niet goed bekend hoe een Ewing-sarcoom ontstaat. Het Ewing-sarcoom is nauw verwant aan de nog zeldzamere Perifere Neuro-Ectodermale Tumor (PNET), die in en rondom het bot voorkomen en de zogenaamde Askin tumor. Samen met de PNET en de Askin tumor vormt het Ewing-sarcoom een groep tumoren die hetzelfde wordt behandeld.
In deze tumoren komt meestal een specifieke afwijking voor in het erfelijk materiaal (DNA), een translocatie (verplaatsing) waarbij delen van twee chromosomen, chromosoom 11 en 22 van plaats verwisselen. Deze afwijking wordt in 90-95% van de tumoren aangetoond. Het Ewing-sarcoom is geen erfelijke ziekte, de afwijking in de genen komt alleen in de tumorcellen voor en niet in de overige lichaamscellen.
Op basis van de ziektegeschiedenis en het lichamelijk onderzoek zijn een aantal diagnostische onderzoeken nodig. Te weten een röntgenfoto en een MRI van de aangedane plek. Met deze beeldvorming wordt gekeken waar de tumor precies zit in het bot, hoe groot de tumor is, hoever de tumor reikt in de omliggende weefsels en hoe de relatie is met de zenuwen en bloedvaten. Uitzaaiingen komen vooral in de longen en botten voor. Daarom wordt een CT scan van de longen gemaakt een PET scan en een MRI van het hele lichaam. Om met zekerheid vast te kunnen stellen dat het om een kwaadaardige tumor gaat is altijd weefsel nodig van de tumor dat wordt weggenomen door middel van een biopsie. De plaats van de biopsie wordt zo gekozen dat het biopsietraject later, bij het wegnemen van de tumor (resectie), kan worden meeverwijderd om achterblijven van kwaadaardige cellen in het biopsietraject te voorkomen.
Bloedonderzoek wordt verricht ter bepaling van de lever, beenmerg en nierfunctie. Bij 1 op de 4 Ewing-sarcoom patiënten worden uitzaaiingen vastgesteld ten tijde van de diagnose.
Welke behandelingen zijn er mogelijk?
De behandeling van een Ewing-sarcoom bestaat uit chemotherapie, een operatie waarbij de tumor wordt verwijderd en meestal radiotherapie (bestraling). Er wordt gestart met een periode chemotherapie (18 weken), soms samen met radiotherapie waarna een operatie volgt. Na deze operatie volgt nog een chemotherapie periode afhankelijk van de respons op de voorgaande chemotherapie. De totale behandeling duurt ongeveer 9 maanden.
Chemotherapie
Vroeger werd een patiënt met een Ewing-sarcoom met chirurgie behandeld, deze bestond vaak uit een amputatie. Deze patiënten overleden bijna allemaal door snel terugkerende ziekte. Dit betekent, zo redeneerde men, dat het Ewing-sarcoom bij diagnose al uitgezaaid was, maar zonder dat er uitzaaiingen te zien waren (micro-metastasering). Op grond hiervan is men begonnen om iedere patiënt met een Ewing-sarcoom te behandelen met chemotherapie. Veel oncologische centra hebben zich beziggehouden om de beste combinatie van chemotherapeutische middelen uit te zoeken. Tegenwoordig wordt er een combinatie van verschillende chemotherapeutische middelen (ook wel cytostatica genoemd) gebruikt:
- Vincristine
- Adriamycine (doxorubicine)
- Ifosfamide
- Cyclofosfamide
- Etoposide
Met deze combinatie behandeling: chemotherapie, chirurgie en radiotherapie is de overleving gestegen naar 55-70%.
Tijdens de chemotherapie wordt regelmatig het effect van de behandeling beoordeeld door middel van controle foto’s, CT thorax, en MRI. Aan de hand van de uitgebreidheid van de tumor en de mogelijkheid om te opereren wordt door het behandelteam besloten hoe de tumor zelf het beste behandeld kan worden, bij voorkeur met operatieve verwijdering. Als dat niet mogelijk is zal de tumor bestraald worden. Na aanpak van de tumor zelf (lokale controle) wordt nog chemotherapie gegeven om restcellen te doden, Deze nabehandeling met chemotherapie varieert van enkele weken tot maanden, afhankelijk van de gekozen nabehandeling.
Omdat het Ewing-sarcoom een zeldzame ziekte is, is het belangrijk om de behandeling te bundelen. Daarom wordt samengewerkt met andere ziekenhuizen en kan behandeling in klinische protocollen worden gegeven. In Leiden heeft het orthopedisch-oncologisch team regelmatig overleg om de behandeling op elkaar af te stemmen. Chemotherapie heeft veel bijwerkingen. De artsen die deze middelen voorschrijven, internist-oncologen, geven uitgebreide uitleg over de gebruikte middelen voordat de behandeling begint. Ondanks preventieve maatregelen kunnen bijwerkingen niet voorkomen worden. Het staat voorop dat de behandeling effectief moet zijn om patiënten met een Ewing-sarcoom een zo groot mogelijke kans op overleving te geven, en daarbij worden een aantal bijwerkingen geaccepteerd.
Radiotherapie
Het Ewing-sarcoom is gevoelig voor de behandeling met radiotherapie (bestraling). Tijdens de bestralingsperiode kan ook chemotherapie gegeven worden. Bestraling kan op verschillende tijdstippen in de behandeling worden ingezet en kan met fotonen of protonen. Er wordt meestal voor de operatie bestraald, het doel is de tumor kleiner te krijgen en kankercellen te doden om een operatie beter mogelijk te maken. Als vooraf duidelijk is dat een operatie niet mogelijk is volgt de bestraling na de chemotherapie.
Radiotherpie heeft bijwerkingen.
Chirurgie
In principe heeft er voor de operatie een periode met chemotherapie en soms radiotherapie plaatsgevonden. Twee weken voor de geplande operatie wordt een MRI gemaakt om te kijken hoe de tumor radiologisch gereageerd heeft op de chemotherapie. Het doel van de operatie is al het tumorweefsel te verwijderen (resectie) met bedekking van het gezonde omringende weefsel waarna het tweede deel van de operatie volgt, het herstellen (reconstructie) van het aangedane lichaamsdeel om een zo optimaal mogelijke functie te behouden. Het type operatie hangt af van de grootte, de lokalisatie en uitbreiding van de tumor in omliggende weefsels zoals spier, gewricht, zenuwen en bloedvaten.
Ledemaat sparende chirurgie
Meestal kan het been of de arm behouden blijven en zal het deel wat verwijderd wordt vervangen worden door:
- donorbot (allograft)
- eigen bot (autograft)
- tumorprothese
Als het gewricht kan worden behouden wordt het defect overbrugd met een gezond stuk bot van uzelf of met donorbot uit de botbank (allograft). Indien er sprake is van het gebruik van donorbot vergt het aan elkaar groeien van de eigen en nieuwe botdelen veel tijd en geduld. Als het defect dicht in de buurt van een gewricht zit (meestal rondom de knie, soms rondom het schouder- of heupgewricht) wordt een kunstgewricht geplaatst. Het voordeel van ledemaat sparende operaties is het behoud van een functioneel been of arm. Het gebruik van een tumorprothese laat snellere belasting toe.
Omkeerplastiek
Wanneer de tumor zich vlak boven de knie bevindt en het onderbeen en de zenuwen tumor vrij zijn dan kan een omkeerplastiek toegepast worden. Nadat de knie en een deel van het bovenbeen zijn geamputeerd, wordt het onderbeen omgekeerd dus met de hiel naar voren en de tenen naar achteren, aan het resterende deel van het bovenbeen vastgezet. De enkel kan dan als kniegewricht fungeren, waaraan een goed functionerende prothese aangemeten wordt.
Amputatie
Wanneer de tumor door zenuwen en bloedvaten groeit en de orthopeed arm of been niet functioneel kan herstellen is amputatie de enige optie.
Wervelkolom en bekken chirurgie
De chirurg streeft ernaar om de tumor in zijn geheel te verwijderen, daarbij neemt hij ook een gedeelte van het niet aangedane weefsel mee. De nauwe relatie met het ruggenmerg en/of wortels maakt het technisch moeilijk om de tumor in zijn geheel te verwijderen. De afgelopen jaren zijn de reconstructieve mogelijkheden sterk verbeterd.
Nadat de keuze voor de operatieve ingreep is gemaakt informeert de fysiotherapeut of verpleegkundig specialist u met foto en videomateriaal over de praktische kanten van de ingreep en het te verwachten revalidatie traject. Op de kindergeneeskunde gebeurt dit samen met een pedagogisch medewerkster. Soms wordt ook een lotgenoot ingeschakeld om mee te praten.
De operatie
De operatie duur is afhankelijk van de plaats en de soort operatie. In de wond wordt meestal een drain achtergelaten, dit is een slangetje waardoor wondvocht afgevoerd kan worden. Na de operatie gaat u naar de uitslaapkamer. Wanneer de lichamelijke controles stabiel zijn gaat u naar de verpleegafdeling. In enkele gevallen is het nodig, afhankelijk van de ingreep, dat u bewaakt wordt op de PACU of Intensive Care.
Na de operatie
Pijn
U kunt pijn hebben aan de wond en eventueel ook aan de spieren, maar deze pijn zal meestal na enkele dagen verdwijnen. Bij een amputatie treedt fantoompijn op. Bij een omkeerplastiek heeft u geen fantoompijn omdat de grote beenzenuw (ischiadicus) niet doorgenomen wordt. De pijnarts regelt de eerste dagen na de operatie de pijnstilling.
Wond
Het wondverband blijft meestal 2 dagen zitten. De wonddrain wordt binnen 2 dagen verwijderd afhankelijk van de wondvocht productie. Er zijn speciale pleisters voor de wond waarmee u kunt douchen. De eerste drie weken na de operatie mag u niet in bad gaan om verweking van de huid te voorkomen. Na 2-3 weken worden de hechtingen op de polikliniek verwijderd.
Katheter
Tijdens de operatie kan een urinekatheter zijn ingebracht. Deze wordt meestal binnen een aantal dagen na de operatie verwijderd.
Uit bed
De operateur bepaalt meestal wanneer u uit bed komt. Dit gaat meestal onder leiding van de fysiotherapeut.
Hoe kunt u zich op de behandeling voorbereiden?
Voorbereiding op chemotherapie
Voor het toedienen van de chemotherapie wordt een centraal intraveneuze katheter gebruikt. Dit wil zeggen dat onder de huid een infuus in een van de grote aders geplaatst wordt die naar het hart toe gaan (meestal in de ondersleutelbeenader). Dit infuus is voor langdurig gebruik en blijft gedurende de behandeling zitten.
Port-a-cath
Dit port-a-cath systeem is speciaal ontworpen om bloedafname en toedienen van medicijnen te vergemakkelijken. Het is een onderhuidse injectiekamer gemaakt van siliconen en titanium. Aan de injectiekamer zit een dunne, siliconen katheter vast. De katheter komt uit in een ader. Met een speciale dunne naald wordt door de huid het siliconen reservoir aangeprikt. De medicijnen of vloeistof gaan via de naald in het reservoir door de katheter en komen direct in de bloedcirculatie. De injectiekamer moet wel steeds worden aangeprikt. De katheter van de Port-A-Cath kan verstopt raken en wordt om dit te voorkomen regelmatig doorgespoten.
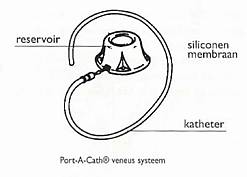
Figuur 1: Port-A-Cath catheter
Cardiologisch onderzoek
Eén van de belangrijkste chemotherapeutische middelen om het Ewing-sarcoom te bestrijden, adriamycine, kan nadelige effecten op de functie van het hart hebben. Om de pompfunctie van het hart te onderzoeken zal een echo of nucleair onderzoek (ejectiefractie) worden verricht. Het echo onderzoek wordt vaker bij kinderen gebruikt, de ejectiefractie bij volwassenen. Na de behandeling wordt de hartfunctie eens in de vijf jaar gecontroleerd en vergeleken met de eerdere metingen.
Voorbereiding op de operatie
Voor de operatie gaat u langs de poli Anesthesie (Link Anesthesie). Indien nodig worden er nog aanvullende onderzoeken gedaan. U wordt opgenomen op de operatiedag (nuchter). Wanneer u medicatie gebruikt bijvoorbeeld pijnstillers of bloedverdunners overleg dan met uw arts of u hiermee moet stoppen. Bij beenoperaties zijn meestal na de operatie krukken nodig. Deze zijn verkrijgbaar bij de thuiszorgwinkel. De fysiotherapeut op de afdeling stelt de krukken voor u af en leert u lopen. Voordat u naar de operatiekamer wordt vervoerd markeert de arts samen met u de geopereerde plek met watervaste stift.
Wat is de prognose?
Genezingskans en prognose
De genezingskans van alle patiënten met een Ewing-sarcoom ligt rond de 55-70%. De genezingskans hangt af of er uitzaaiingen van de tumor op andere plaatsen zijn, de plaats waar de tumor zich bevindt in het skelet of weke delen, de grootte van de tumor en de leeftijd van de patiënt. Een andere voorspellende factor is de reactie van de tumor op de chemotherapie. Dit wordt door de patholoog beoordeeld in het weefsel dat bij de operatie is verwijderd. Men spreekt van een goede respons als er minder dan 10% vitale tumorcellen wordt gevonden.
Terugkijkend naar de vroegere behandelingen met chemotherapie was er een genezing van 24%-50%. Met meer efficiënte therapieën in studieverband, zoals die ook in het LUMC worden gegeven, worden tegenwoordig overlevingspercentages tot 55%-70% behaald. Omdat elke situatie en elke persoon uniek is, blijft het moeilijk voorspellingen te doen.
Wat zijn de risico's, bijwerkingen of complicaties?
Bijwerkingen chemotherapie
Hartfunctie
Eén van de belangrijkste chemotherapeutische middelen om het Ewing-sarcoom te bestrijden, adriamycine, kan nadelige effecten op de functie van het hart hebben. Om de pompfunctie van het hart te onderzoeken zal een echo of nucleair onderzoek (ejectiefractie) worden verricht. Het echo onderzoek wordt vaker bij kinderen gebruikt, de ejectiefractie bij volwassenen. Na de behandeling wordt de hartfunctie eens in de vijf jaar gecontroleerd en vergeleken met de eerdere metingen.
Nierfunctie
De nieren zorgen voor de uitscheiding van afvalproducten in ons lichaam. Door ifosfamide kunnen de nieren beschadigd worden, waardoor de uitscheidindings functie verminderd. Over het algemeen gebeurt dat alleen bij een hogere totaaldosis, maar de nieren worden regelmatig gecontroleerd of er ook bij lagere dosis niet al een probleem optreedt met de nierfunctie.
Haarverlies
Door de chemotherapie valt ongeveer drie weken na de eerste kuur het hoofdhaar uit. Er kan gebruik gemaakt worden van een pruik of andere hoofdbedekking zoals sjaal of pet. Haaruitval kan gepaard gaan met een gevoelige of een pijnlijke hoofdhuid. Ook kunnen wenkbrauwen, wimpers, oksel-, lichaams- en schaamharen uitvallen. Haaruitval is tijdelijk, ongeveer een maand na het beëindigen van de chemotherapie begint het haar weer te groeien. Dit kan in het begin verschil vertonen met het oorspronkelijke haar.
Maag/darmklachten
Door de chemotherapie kan men last krijgen van verminderde eetlust, een vol gevoel, opboeren, zuurbranden, misselijkheid en braken. Tijdens de chemotherapie worden medicijnen tegen de misselijkheid gegeven en ook voor de eerste dagen na de kuur. Er wordt geadviseerd om regelmatig kleine maaltijden te gebruiken en goed te drinken.
Beenmergeffecten
Door chemotherapie kan er remming zijn van de aanmaak van nieuwe bloedcellen. Deze remming kan een anaemie (tekort aan rode bloedcellen, dit geeft bloedarmoede), leucopenie (te weinig witte bloedcellen) en/of trombocytopenie (te weinig bloedplaatjes) veroorzaken. Rode bloedcellen zorgen voor het vervoer van zuurstof. Symptomen van anaemie kunnen zijn: bleekheid, duizeligheid, hoofdpijn, hartkloppingen, kortademigheid, vermoeidheid, koud voelen. Witte bloedcellen zorgen voor bescherming tegen infecties. Controleer wondjes op roodheid, pijn en zwelling. Zorg voor goede lichaamshygiëne en goede mondverzorging.
Bloedplaatjes zorgen voor de stolling (stoppen van een bloeding). Er is een verhoogde kans op een neusbloeding, blauwe plekken en bloed bij plassen of hoesten. Een menstruatie kan meer bloedverlies geven dan voorheen.
Mondslijmvlies
Door de chemotherapie kan er irritatie, beschadiging of ontsteking van het mondslijmvlies en tandbederf optreden. Veranderingen aan het mondslijmvlies kunnen zijn: droge mond, gevoeligheid bij het eten of drinken van zure of gekruide spijzen en dranken, gevoeligheid voor de temperatuur van eten en drinken, slechte adem, snel bloedend tandvlees en taai speeksel. Het is belangrijk dat de mondholte goed verzorgd wordt.
Perifere zenuwstelsel
Door de chemotherapie kan er een tintelend of doof gevoel in de vingertoppen, voetzolen of tenen optreden. Dit kan soms tot 1 jaar na de chemotherapie. Koude kan deze klachten verergeren.
Vruchtbaarheid en seksualiteit
Door de chemotherapie kan de vrouw veranderingen in haar menstruatiepatroon bemerken. De menstruatie kan heviger/onregelmatiger worden of tijdelijk verdwijnen. Dit kan gepaard gaan met overgangsklachten. Na het beëindigen van de chemotherapie herstelt het menstruatiepatroon zich meestal weer. Bij de man kan het soms 5 jaar duren voor de aanmaak en kwaliteit van het sperma weer hersteld is. Chemotherapie kan beschadiging van eicellen of zaadcellen veroorzaken, daarom moet een zwangerschap tot enkele maanden na de chemotherapie worden voorkomen. Het is noodzakelijk om door te gaan of te starten met een betrouwbare methode van anticonceptie. Chemotherapie hoeft geen belemmering te zijn voor geslachtsgemeenschap, wel kan het slijmvlies van de vagina droger worden. De behoefte aan seksueel contact kan door vermoeidheid/zwakte afnemen. Afvalstoffen komen in zeer kleine hoeveelheden in het sperma voor, dit is niet schadelijk voor de partner.
Invriezen sperma voor later gebruik
De testikels (zaadballen), de plaats waar de zaadcellen worden aangemaakt, kunnen door de chemotherapie ook aangetast worden. Dit kan tijdelijke of blijvende onvruchtbaarheid veroorzaken. Daarom is het voor patiënten die een vruchtbaarheidsbedreigende behandeling zullen ondergaan aan te raden om sperma in te vriezen om eventueel later te gebruiken.
Cryopreservatie van de eierstok
Cryopreservatie van de eierstok (ovarium) wordt in verschillende universitaire ziekenhuizen toegepast. Tijdens een kijkoperatie (laparoscopie) wordt één van de 2 eierstokken weggehaald en ingevroren in de vloeibare stikstof. Wanneer na de chemotherapie blijkt dat de vrouw onvruchtbaar is op grond van onwerkzame eierstokken, kan de ingevroren eierstok teruggeplaatst worden. Deze vorm van bewaren van de vruchtbaarheid wordt aangeboden aan meisjes/ vrouwen die al met de menstruatie begonnen zijn.
Mogelijke complicaties van de operatie
Wondinfectie
De kans hierop is relatief groot, dit komt door de grootte van de ingreep, het gebruik van niet lichaams eigen materiaal en omdat de afweer door de chemotherapie meestal minder is. Wanneer een wondinfectie optreedt gebeurt dit vaak binnen een week. Wondinfecties zijn zichtbaar door roodheid en/of pijn aan de wond en door temperatuurverhoging. Behandeling kan bestaan uit rust, antibiotica en soms operatief. Indien er verdenking is op een wondinfectie moet u contact op nemen met de afdeling orthopedie (dienstdoende orthopeed).
Trombose
Alle mensen die een langdurige operatie ondergaan aan één van de ledematen hebben meer kans op het krijgen van trombose (aderverstopping door een bloedstolsel). Om dit te voorkomen krijgt u vanaf de operatie bloedverdunnende medicijnen in injectievorm gedurende een periode van 6 weken. Een trombosebeen kan zelfs ontstaan bij gebruik van deze medicijnen.
Beschadiging van een zenuw
Tijdens de operatie kan een zenuw opgerekt, bekneld raken of afhankelijk van de soort operatie doorgenomen worden.
Loslaten van de prothese
Soms kunnen prothesen loslaten en is een nieuwe operatie meestal noodzakelijk.
Meedoen aan wetenschappelijk onderzoek
Er hebben in het verleden verschillende basale en klinische studies plaats gevonden. Gezien het concentreren van patiënten met een Ewing-sarcoom over vijf centra ligt het in de lijn der verwachting dat er in de toekomst meerdere wetenschappelijke studies zullen plaats vinden.
Welke specifieke nazorg kunnen we bieden bij deze aandoening?
Medische nazorg/ follow-up
Steeds meer patiënten met kanker overleven, door verbeterde diagnostiek en behandelingsmethoden. Dit is een mooie vooruitgang, maar deze heeft ook een keerzijde. Bij een deel van de patiënten blijken er late effecten van de behandeling voor te komen. Deze effecten kunnen variëren van specifiek lichamelijk tot psychosociaal. Van het medicijn Adriamycine bijvoorbeeld weten we inmiddels dat dit op latere leeftijd hartschade kan veroorzaken. Maar er kunnen ook leer- en aandachtsproblemen ontstaan of problemen op het gebied van de vruchtbaarheid en de groei. Deze “late” effecten kunnen de kwaliteit van leven beïnvloeden, en soms ook verdere medische zorg noodzakelijk maken. Om deze redenen blijft u jarenlang onder controle. De eerste jaren intensief en later jaarlijks.
Fysiotherapie / revalidatie
Afhankelijk van de operatieve ingreep wordt snel na de operatie gestart met de revalidatie behandeling. Gedurende de postoperatieve chemotherapie wordt deze behandeling vooral uitgevoerd en gecoördineerd vanuit het ziekenhuis, soms wordt ook een fysiotherapeut in de eigen woonplaats bij de behandeling betrokken.
Indien een donorbot reconstructie is verricht, wordt het been gedurende een periode van 6 - 12 maanden met behulp van een koker of brace beschermd. De revalidatie na de operatie met de chemotherapie duurt zes maanden tot een jaar. Zware fysieke arbeid of belastende sporten, zoals skiën, paardrijden of voetballen zijn voor patiënten met een reconstructie beperkt mogelijk. Fietsen, wandelen, golfen of zwemmen, kunnen bijvoorbeeld wel. Na een tumorprothese reconstructie is een brace of koker meestal niet nodig en enkele weken na de operatie kan de prothese belast worden.
Bij een amputatie van (een deel van) het been wordt na het verwijderen van het stompgips enkele dagen na de operatie gestart met het zwachtelen van de stomp. Staan en lopen gebeurt op de afdeling onder leiding van de fysiotherapeut.
Na enkele weken komt de prothesemaker en kan als de prothese klaar is gestart worden met de prothese training. De revalidatie na een amputatie start al kort na de ingreep en afhankelijk van de hoogte van de amputatie is zware belasting en sport mogelijk. Vooral jongere patiënten worden gestimuleerd om actief aan sport te gaan doen. Zij worden geïnformeerd over sportactiviteiten zoals skiën op één been en atletiek. De revalidatie en het aanmeten van een prothese na een omkeerplastiek start na enkele weken. Met deze prothese is een goed looppatroon mogelijk evenals zware belasting en sport. Bij patiënten met wervelkolom en / of bekken chirurgie wordt een direct belastbare situatie nagestreefd, soms is ondersteuning met een gipscorset of gipsbroek nodig.
Jong en Kanker
Het Ewing-sarcoom komt meestal voor bij kinderen en jong volwassenen, Adolescent & Young Adults (AYA's).
Als je als jong volwassene kanker krijgt, staat je wereld op z'n kop. Je ziekte en de behandeling brengen veel vragen met zich mee. Over je ziekte, maar bijvoorbeeld ook over studie, werk, kinderwens, hypotheken, relaties en seks.
Met al deze vragen kun je terecht bij het AYA-team van het LUMC. Dit team biedt zorg en ondersteuning aan alle jongvolwassenen die in de leeftijd van 16-35 jaar kanker hebben of hebben gehad.
Behandelteam
Iedere patiënt met een Ewing-sarcoom wordt behandeld door een multidisciplinair behandelteam met veel ervaring in de behandeling van deze zeldzame aandoening. Er zijn vijf behandelteams in Nederland actief, te weten; AMC in Amsterdam, UMCG in Groningen, UMCN Radboud in Nijmegen, het Prinses Maxima Centrum in Utrecht (kinderziekenhuis gespecialiseerd in kinderoncologie) en het LUMC in Leiden. Het team bestaat o.a. uit een (kinder)oncoloog, orthopeed, radioloog, patholoog, radiotherapeut, (thorax)chirurg, neurochirurg, revalidatiearts, fertiliteitstarts, plastisch chirurg, orthopedisch instrumentmaker, maatschappelijk werk, psycholoog, fysiotherapeut, pedagogisch medewerker, oncologie verpleegkundige en verpleegkundig specialist.
Aangezien de afwijking in het bot zit is het eerste contact in het ziekenhuis meestal via de orthopeed. Gedurende het behandeltraject is het multidisciplinaire team permanent bij de behandeling betrokken. De hoofdbehandelaar wisselt afhankelijk van het stadium waarin de patiënt zich bevindt, bijvoorbeeld tijdens de chemotherapie is dit de internist-oncoloog, tijdens de chirurgie de orthopeed, tijdens de radiotherapie de radiotherapeut. Het beleid wordt tijdens het wekelijkse multidisciplinair overleg besproken.
Contact
Telefoonnummers
LUMC, algemeen: 071-5269111
Polikliniek Orthopaedie: 071-5268003 (te bereiken op werkdagen tussen 09.00 en 12.30 uur)
Verpleegafdeling Orthopaedie: 071-5262099 / 071-5262065